АКЦІЇ! ПЕРЕГЛЯНУТИ ПОВНИЙ ПЕРЕЛІК ДОСТУПНИХ ПРОПОЗИЦІЙ МОЖНА ТУТ
Категорії новин:
Погляд на нові біомаркери географічної атрофії
Мультимодальна візуалізація є стандартом для діагностики сухої форми ВМД, що потрібно знати.
ВМД — це багатофакторне захворювання, яке включає нечітко визначену взаємодію між старінням, генетикою та факторами навколишнього середовища, пов’язаними з окислювальним стресом, запаленням і порушенням функціонування позаклітинного матриксу в сітківці, переважно в макулі. Класифікація ВМД — традиційно прив’язана до наявності та розміру друз і наявності пігментних змін або інших ознак атрофії — забезпечує прогностичну оцінку прогресування захворювання. На відміну від ранньої ВМД, проміжна ВМД (iAMD) має вищу швидкість прогресування до пізньої ВМД, що визначається як розвиток географічної атрофії (GA) або субфовеальної макулярної неоваскуляризації (MNV). Дослідження показало, що 5-річний ризик прогресування до піздньої ВМД становив 0,4% для очей без великих друз або пігментних аномалій і 47% для очей з двосторонніми великими друзами та пігментними аномаліями.
Для лікування географічної атрофії (GA) тепер має схвалення препарат пегцетакоплан (Syfovre, Apellis Pharmaceuticals). Проводяться значні дослідження для кращого розуміння потенційної парадигми лікування пацієнтів з проміжною ВМД (iAMD) особливо для відбору пацієнтів з візуалізаційними ознаками високого ризику прогресування до пізньої ВМД. Таким чином, клініцисти повинні мати можливість ідентифікувати пацієнтів з iAMD, які мають високий ризик для прогресування.
Новий стандарт для відображення ВМД
У той час як офтальмоскопія та кольорова фотографія очного дна були стандартом для обстеження та визначення стадії ВМД, прийняття інших методів візуалізації, таких як фундус – автофлуоресценція (FAF), обстеження в ближньому інфрачервоному діапазоні (NIR) та ОКТ, стало основою для групи класифікації атрофії - Classification of Atrophy Meeting (CAM) для оновлення визначення стадій ВМД та прогнозу прогресування. Мультимодальна візуалізація має бути загальноприйнятою для правильної діагностики та прогнозування ВМД.
При застосуванні метода оптичної когерентної томографії (ОКТ) в якості його переваг особливо підкреслюється здатність до:
- забезпечення більшої точності оцінки сітківки в об'ємному вигляді, враховуючи високу осьову роздільну здатність;
- незалежного оцінювання кожного шару сітківки та виявлення ранніх ознак патології;
- створення зображення en face, яке можна використовувати для демаркації меж атрофії та прямого співвіднесення з іншими методами візуалізації;
- забезпечити необхідну кількість сканів за один візит.
Друзи та гіперрефлективні фокуси
При дослідженні зображень ОКТ оцінювали класичні фактори ризику прогресування ВМД, такі як друзи і пігментні зміни, що візуалізуються на ОКТ як гіперрефлективні фокуси (HRF). Виявлений підвищений ризик прогресування при збільшенні базової площі і об’єму друз, а також наявності гіперрефлективних фокусів.
Очі з об’ємом друз щонайменше 0,03 мм3 мали чотириразове підвищення ризику розвитку макулярної неоваскуляризації (MNV) або географічної атрофії (GA) протягом двох років, та п’ятикратне підвищення ризику розвитку географічної атрофії GA протягом двох років при наявності гіперрефлективних фокусів (HRF) порівняно з очима без базових HRF.
Ретикулярні псевдодрузи та кальцифіковані друзи
Ретикулярні псевдодрузи (RPD), також відомі як субретинальні друзеноїдні відкладення, які зазвичай зустрічаються у верхніх областях макули та становлять підвищений ризик прогресування ВМД.
Поширеність RPD (найкраще відображається за допомогою NIR-зображення) змінюється залежно від стадії ВМД, з найвищою поширеністю в очах з проміжною ВМД (62,6%). Крім того, наявність ретикулярних псевдодруз була пов’язана з майже втричі підвищеним ризиком прогресування до пізньої ВМД.
Кальцифіковані друзи (CaD) поширені в стадії проміжної ВМД та мають високу прогностичну цінність для розвитку пізньої ВМД.
Гетерогенна внутрішня рефлективність в друзах (викликана мультилобулярними вузликами кристалічного фосфату кальцію) була присутня в 45% очей з проміжною ВМД та асоціюється з розвитком пізньої ВМД протягом одного року (співвідношення шансів: 6,36). 42.7% очей з проміжною ВМД мають CaD та більшість розвиваються в області географічної атрофії, таким чином CaD слід враховувати при оцінці ризику ВМД.
Визначення атрофії на ОКТ
Так як зазвичай географічна атрофія виявлялася за допомогою кольорової фотографії очного дна, групою класифікації CAM розроблено нову номенклатуру для класифікації атрофій, пов’язаних з ВМД на базі ОКТ обстежень: неповний пігментний епітелій сітківки (RPE) та зовнішня атрофія сітківки (iRORA) і повний RPE та зовнішня атрофія сітківки (cRORA, рис.1). cRORA відповідає площі щонайменше 250 мкм на одному горизонтальному В-скані, що відображається в наступному:
1. зменшення або повна втрата RPE,
2. відповідний дефект гіпертрансмісії (hyperTD) через область змін RPE
3. ознаки дегенерації фоторецепторів, такі як осідання внутрішнього ядерного шару (INL) або зовнішнього плексиформного шару; витончення зовнішнього ядерного шару; наявність гіпорефлективних клинів в шарі волокон Генле; або порушення зовнішньої обмежувальної мембрани (ELM) або еліпсоїдної зони (EZ), все за відсутності розриву RPE.
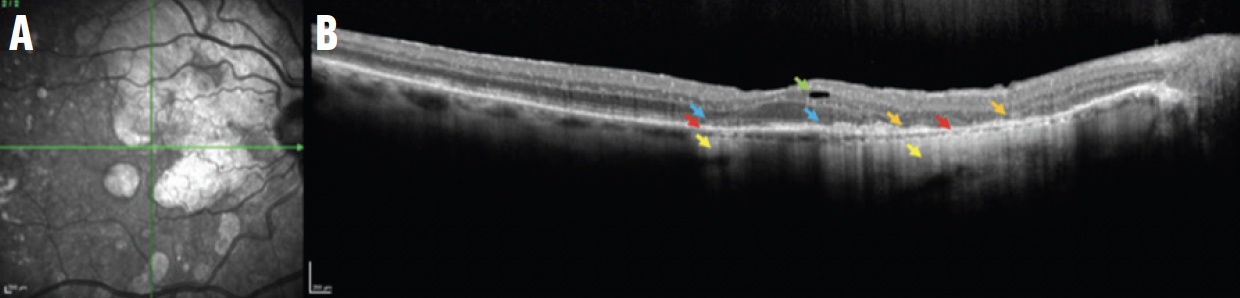
Рис. 1. Зображення в ближньому інфрачервоному діапазоні (NIR) (A) та В-скан ОКТ cRORA ураження (B) відображають порушення ELM and EZ (сині стрілки) та ділянки зменшення RPE (червоні стрілки) з гіпертрансмісією в хоріоїдею (жовті стрілки). Є ділянки дегенерації фоторецепторів (помаранчеві стрілки) і дегенеративна кіста (зелена стрілка).
iRORA відноситься до області горизонтального В-скану, що має деякі особливості cRORA (рис. 2 та 3).
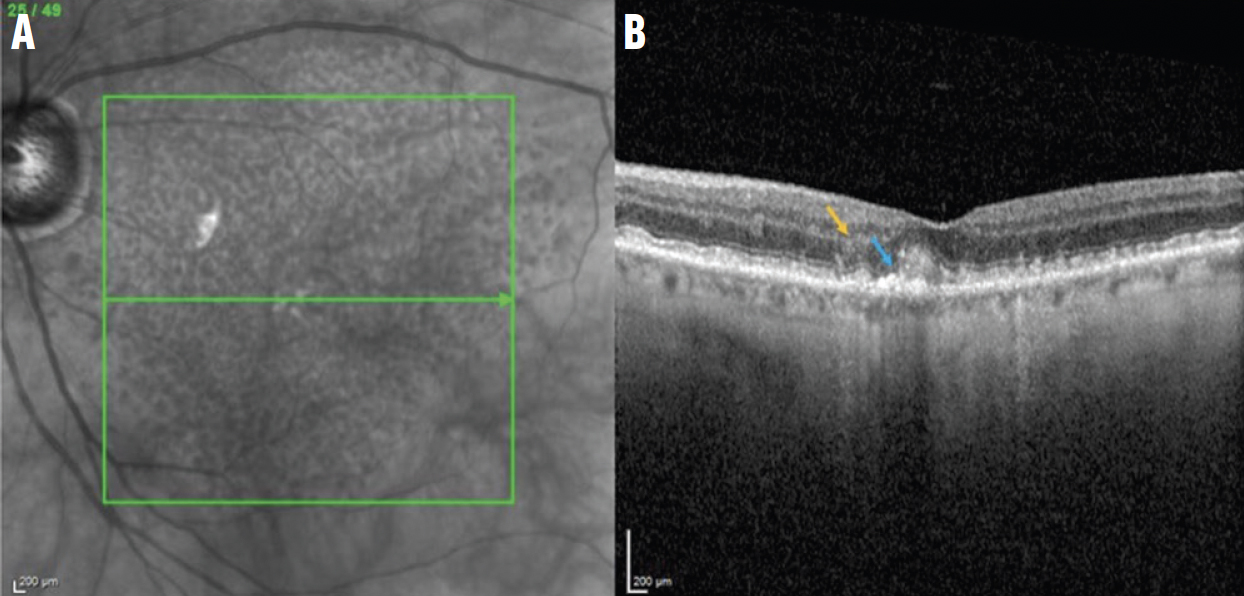
Рис. 2. NIR зображення (A) та B-скан ОКТ iRORA ураження (B) відображають порушення ELM та EZ (сині стрілки) та осідання внутрішнього ядерного шару INL (помаранчеві стрілки).
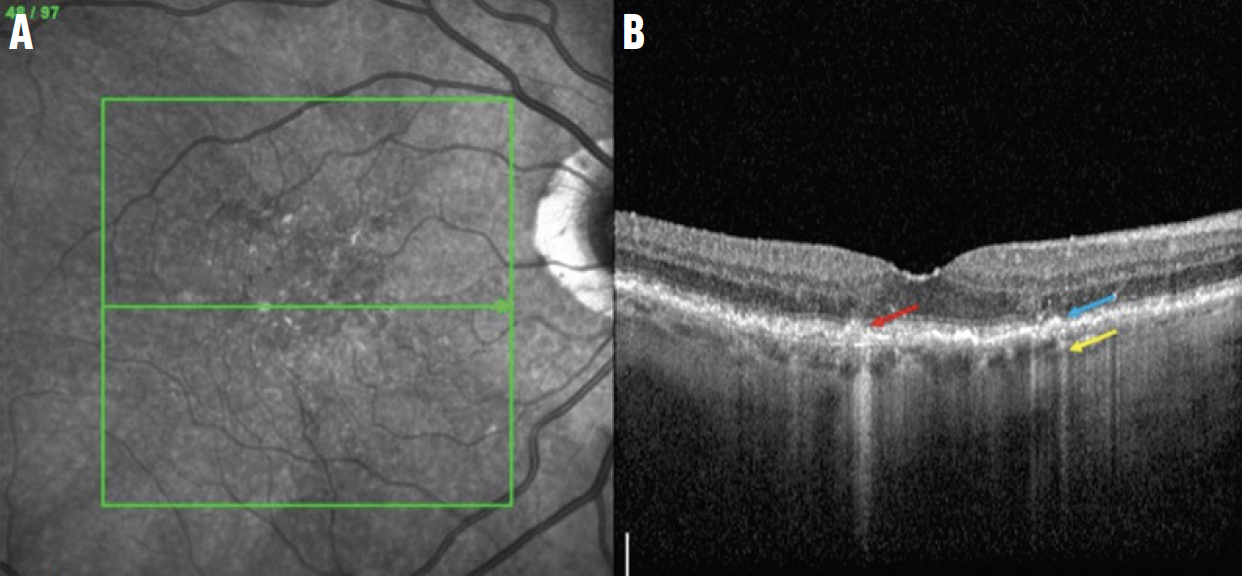
Рис. 3. NIR зображення (A) та В-скан ОКТ iRORA ураження (B) відображають порушення ELM та EZ (сині стрілки) та вогнищеве зменшення RPE (червона стрілка) з гіпертрансмісією в хоріоїдею (жовта стрілка).
Дослідники працюють над визначенням корисності виявлення уражень iRORA та оцінюванням ризику прогресування до cRORA на ОКТ та/або географічної атрофії (GA) на кольоровому фото очного дна.
Особливості iRORA означають підвищений ризик прогресування до cRORA. Наприклад, було виявлено, що приблизно 93% уражень iRORA перетворюються на cRORA протягом 24 місяців, тоді як ушкодження iRORA перетворюються в GA, що фіксується на кольоровому фото очного дна, зі швидкістю приблизно 3% протягом 24 місяців і 10% прогягом 30 місяців.
Іншою ознакою, що попереджає про географічну атрофію на ОКТ є виявлення гіпорефлективних клинів в шарі волокон Генле та/або осідання внутрішнього ядерного шару та зовнішнього плексиформного шару з/або без змін в RPE або гіпертрансмісії. Зародки географічної атрофії (nGA) мали набагато більший коефіцієнт конверсії до GA на фото очного дна ніж iRORA протягом 24 місяців (38% проти 3%).
Атрофію можна побачити набагато раніше на OКT, ніж на кольоровому фото очного дна, і nGA має більш специфічні критерії, ніж iRORA. Таким чином, ці результати показують, що iRORA перетвориться на cRORA (тобто справжню необоротну атрофію сітківки) за відносно короткий час, але може залишатися непоміченою на фото очного дна набагато довше.
Крім того, iRORA може означати, що необоротне пошкодження функцій вже відбулось (тобто, iRORA та пов’язані зміни зору можуть бути клінічно схожі з cRORA). Багато уражень cRORA помилково відносять до категорії iRORA, оскільки критерії діагностики iRORA не враховують всі розміри атрофічних уражень, область атрофії має відповідати критеріям cRORA, якщо вертикальні та діагональні В-скани співвідносяться з горизонтальними В-сканами.
Гіпертрансмісія на En Face
Як альтернатива iRORA/cRORA, визначеним за допомогою ОКТ, гіпертрансмісії у хоріоїдеї — видимі як світлі ділянки на зображеннях ОКТ en face, розташовані в сегменті з межами від 64 мкм до 400 мкм під мембраною Бруха — забезпечують надійну, відтворювану та незалежну характеристику і є фактором ризику для географічної атрофії.
Порівняно з критеріями класифікації iRORA/cRORA, класифікація гіпертрансмісії за допомогою зображень en face дозволяє: вимірювати найбільший лінійний розмір ураження у будь-якому векторі (не лише горизонтально), пряме візуальне порівняння з іншими методами візуалізації ВМД, такими як кольорове фото очного дна, обстеження в ближньому інфрачервоному світлі та фундус-автофлуоресценції і швидку оцінку всієї області сканування.
Дослідження показують, що гіпертрансмісії з найбільшим лінійним розміром принаймні 250 мкм, ймовірно, зберігатимуться протягом 3-х років, сильно корелюють з зародковою географічною атрофією (79%) і означають 80-кратний ризик утворення cRORA протягом 3 років. У той час як було виявлено, що гіпертрансмісії менших розмірів є тимчасовими та не настільки сильно корелюють із розвитком атрофії, вони все одно можуть означати зони ризику RPE, оскільки ці області можуть кваліфікуватися як iRORA.
Оцінка ризику після GA
Після того, як iRORA/cRORA, nGA або гіпертрансмісії утворяться в оці, у тому самому оці та іншому оці, ймовірно, розвинуться додаткові ушкодження.
Крім того, при розвитку географічної атрофії, на ОКТ та/або на кольоровому фото очного дна, певні характеристики (тобто більші ураження, мультифокальність і екстрафовеальна локалізація) пов’язані зі збільшенням швидкості росту. Примітно, що хоча субфовеальні ураження географічної атрофії можуть корелювати із значними падіннями гостроти зору, зорова функція знижується до того, як буде діагностовано ураження фовеа, і існує велика варіація в гостроті зору, навіть якщо візуалізація свідчить про значне порушення гостроти зору. Тому гострота зору не є надійним показником тяжкості захворювання.
Нарешті, як рекомендувала група CAM, дослідження методом фундус-автофлуоресценції може також надати додаткову інформацію, щодо оцінки ризику. У той час як географічна атрофія відповідає гіпоавтофлуоресценції, темпи росту географічної атрофії відрізняються залежно від ступеня та характеру гіперавтофлуоресценції. Відсутність гіперавтофлуоресценції або фокальних патернів гіперавтофлуоресценції пов’язані з повільними темпами росту географічної атрофії (0,38–0,81 мм2/рік), дифузні та смугасті моделі мають більш ніж удвічі більші темпи росту (1,77–1,81 мм2/рік), а підтип «дифузно-краплинний» має найвищу швидкість росту (3,02 мм2/рік). Крім того, ступінь гіперавтофлуоресценції навколишніх уражень географічної атрофії, що представляють групу ризику, позитивно корелює зі швидкістю зростання географічної атрофії.
Автори:
Фархан Е. Хія, доктор медичних наук
Клінічний науковий співробітник, захворювання сітківки, Інститут зору Баскома Палмера, Медична школа Університету Маямі Міллера, Маямі f.hiya@miami.edu Розкриття фінансової інформації: немає
(Farhan E. Hiya, MD Clinical Research Fellow, Retinal Diseases, Bascom Palmer Eye Institute, University of Miami Miller School of Medicine, Miami f.hiya@miami.edu Financial disclosure: None)
Абрахім Ахмед, студент-медик, Медичний коледж Морсані, Університет Південної Флориди, Тампа, Флорида abrahim@usf.edu
Фінансова інформація: немає
(Abrahim Ahmed, BS Medical Student, Morsani College of Medicine, University of South Florida, Tampa, Florida abrahim@usf.edu Financial disclosure: None)
Девід А. Ейхенбаум, доктор медичних наук
Директор з досліджень, Асоціація Флориди по сітківці та скловидному тілу, Санкт-Петербург, Флорида. Співпраця: доцент, Медичний коледж Морсані, Тампа, Флорида deichenbaum@rvaf.com Розкриття фінансової інформації: консультант/доповідач (Apellis Pharmaceuticals)
(David A. Eichenbaum, MD
Director of Research, Retina Vitreous Associates of Florida, Saint Petersburg, Florida Collaborative Associate Professor, Morsani College of Medicine, Tampa, Florida deichenbaum@rvaf.com Financial disclosure: Consultant/Speaker (Apellis Pharmaceuticals))
- Tags:
- Корисні статті
- Офтальмологія
Останні новини та події
